A következőkben, a természetben előforduló két olyan molekulát modellezünk és vizsgálunk meg, amelyek az emberi szervezetbe jutva sorozatosan átalakulnak, és ennek során fejtik ki hatásukat. Az átalakulás során megdöbbentő módon, olyan fázisokon is átmennek, amelyek más, az emberi szervezetre szintén hatással levő molekulákkal mutatnak morfológiai azonosságot. Azonban nem csak morfológiai az azonosság. A hatásuk is szinte teljesen azonos, tehát alappal feltételezhető, hogy a szervezetnek ugyanazon receptorain keresztül hatnak, és hatásmechanizmusuk is azonos lehet.
A molekulák morfológiai modelljét az Avogadro kémiai modellező szoftver segítségével állítottuk elő, amely lehetővé teszi a modell körbeforgatását. Így több oldalról is szemügyre vehetjük, amely segíti az összehasonlítást. Azok számára, akik nem rendelkeznek ezzel a szoftverrel, a modelleket kép formájában is bemutatjuk, de a jobb megértés kedvéért javasoljuk az Avogadro letöltését. Innen ingyenesen letölthető: http://avogadro.en.softonic.com/.
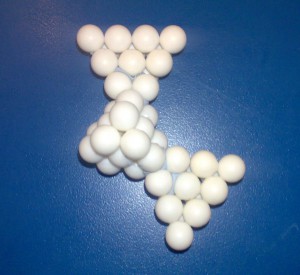
Az első molekula a metil-alkohol (metanol, hidroxi-metán) amelynek szerkezeti képlete a konvencionális kémia szerint CH3OH, amely nem elemi összefüggés, hanem egy kémiai következtetés eredménye. A morfológiában ezért ezt nem alkalmazhatjuk ebben a formában, csak a következtetése nélkül, azaz az összetevők tömegszámának és darabszámának megfelelően így: O, C, H4. A morfológiai alapú következtetést majd a modell megalkotása után tudjuk levonni, és azt összevetni a hagyományos kémiai képlettel és elnevezéssel.
A modellezést az oxigén és a szén legegyszerűbb kapcsolódásának bemutatásával kezdjük, majd megnézzük, hogy az átalakítható-e, és ha igen, hogyan. Az egy oxigén egy szén kapcsolódása a természetben a szénmonoxid molekulában fordul elő. Lássuk tehát először ennek a modelljét. Kép + Avogadro fájl
Láthatjuk, hogy noha a kötés morfológiai szempontból lapkötés, amellyel egytest jön létre (tehát a molekula gáz lesz), a kötéssel egyúttal az oxigén egyik hidrogénkötő helye is kapott egy protont, azaz az oxidációs aktivitása valamivel gyengébb lesz. Azt is láthatjuk, hogy ezt a modellt ugyan kiegészíthetnénk négy protonnal, de csak úgy, ha az oxigénen helyezünk el hármat (kiegészülés), amely ekkor formailag neonná válna, és a szénen csak a morfológiai összefüggésekkel ellentétesen tudnánk elhelyezni a negyedik protont. Ez pedig nemcsak a morfológiai összefüggésekkel lenne ellentétes, de a metilalkohol (vízzel jól elegyedő, kis viszkozitású folyadék, és jó oldószer) fizikai tulajdonságait sem kielégítő modell lenne.
A vízzel jól elegyedő, kis viszkozitású, jó oldószer folyadékokat olyan kötések jellemzik, amelyek könnyen felbomlanak, majd újra összezárnak, és maguk közé képesek fogadni arra alkalmas más molekulákat, továbbá, molekuláris kötéseik képesek elfordulni anélkül, hogy elengednének. A morfológiában ezeknek a feltételeknek az egyes-hármas (gömbcsukló) kötés felel meg, a kémiában pedig a hidrogén-híd kötés.
A modellezés során tehát olyan formát és kapcsolódást kell találnunk, amely alkalmas más molekulákkal lánccá és térhálóvá való kapcsolódásra is, de a formai kiegészülés összefüggésének is megfelel. Ezt a formát akkor kapjuk meg, ha a szenet metánná egészítjük ki a 4 protonnal. Ekkor a következő formát kapjuk, amelyről látható, hogy az oxigénnel képes kötést létesíteni, hogy az vele molekulát alkosson, és molekulává alakulás után is marad két olyan csúcsa, amellyel további metanol molekulák oxigénjéhez is képes hídkötéssel kapcsolódni. Így sok ilyen molekula valódi folyadékot képes alkotni.
Kép – metán
Kép – Oxigén 16
Kép – metanol
A képekről láthatjuk, hogy a modell alakja megfelel egy metán molekula és egy oxigén atom kapcsolatának. Morfológiailag ezért a molekula elnevezése metán monoxid lenne. Ez csak kis mértékben tér el azoktól a kémiai elnevezésektől, amelyekben a metán szó szerepel, amely egyértelműen utal arra, hogy egy szén és négy proton kapcsolódásáról van alapvetően szó. A modell éppen ezt képezi le. A különbség azonban nagy. A modellről azt láthatjuk, hogy egy oxidról van szó, amely csak formailag hidroxid, hiszen egyetlen proton sem tartozik egészében az oxigénhez, hanem az a metánnak az egyik protonjához is kapcsolódik, azaz a molekula összetevői osztoznak azon a protonon.
Nézzük tovább, hogy mi történik akkor, amikor ez a molekula az ember szervezetébe tömény folyadék részeként bekerül. Úgy tudjuk, hogy oxidációja során formaldehid keletkezik, amely a metán oxidációjának is a terméke, tehát az általunk alkotott molekula nem csak formailag tartalmaz metánt, de valószínűleg a valóságban is. A formaldehid konvencionális kémiai szerkezeti képlete CH2O, amely morfológiailag O, C, H2. Ugyanakkor a formaldehidről úgy tudjuk, hogy gáz, és azt is, hogy többnyire egy köztes vegyület a metán és egyes szerves vegyületek oxidációs sorában. Alakítsuk ki az ezeknek a feltételeknek megfelelő gázmolekulát a metán monoxidunkból.
Kép + Avogadró fájl
Íme, a formaldehid molekulája. Döbbenetes a változás. Az eredeti metánunk többé nem metán, mert elvesztette két protonját, amelyek egy külső oxigénhez kapcsolódva vízmolekulát alkottak és eltávoztak a vegyületből. Így viszont formájában a nitrogén 14-es tömegszámú izotópjával lett azonos, amely gáz. Az oxigénjéhez való kapcsolódása is megváltozott. Újra egytestet alkot vele, tehát gázként fognak együtt viselkedni. Formájában a molekula teljesen olyan lett, mintha nitrogén monoxid molekula lenne. A molekula egyúttal nagyon hasonlít a bevezetőben bemutatott szénmonoxid modellhez. Tehát feltehetőleg úgy is hat a szervezeten belül, mint a szénmonoxid.
Mivel a formaldehid (vagy más néven metil aldehid, vagy metilén-oxid) csak köztes oxidációs termék, nézzük meg, hogy hogyan fejlődik tovább az oxidációs átalakulás folyamatában, az emberi szervezeten belül.
Úgy tudjuk, hogy a formaldehidből további oxidációval hangyasav keletkezik, amely a modellje alapján formailag teljesen azonos a nitrogén dioxiddal, amely viszont a széndioxidhoz formailag nagyon hasonló modell. Annál csupán két protonnal kevesebb, amint azt a következő ábrákon láthatjuk. A két proton ráadásul nem a molekula aktív felszínén van, vagy onnan hiányzik, tehát a két molekula aktív összetevője, az oxigén ugyanolyan módon képes hatni, mint addig. Feltehető, hogy a szervezet össze is téveszti a két molekulát.
Kép + Avogadro modell
Az eddigiekből következik, hogy amennyiben a modell helyes, akkor a metanol az emberi szervezetben ugyanazt a hatást fejti ki, mintha előbb szénmonoxidot lélegezne be az ember, amely a vérben az oxigén helyét foglalja el. A maradék monoxid pedig tovább oxidálódva széndioxidhoz hasonló (hatásában is) vegyületté alakulna, amely nagy mennyiségben szintén az oxigén arányát csökkenti a szervezetben (a vérben). Feltehető tehát, hogy bizonyos mennyiség feletti metanol elfogyasztása esetén az ember valójában oxigénhiányban hal meg, mintha szénmonoxid mérgezése lenne. Mivel az agy a legnagyobb oxigénfogyasztó, az agykárosodás szinte elkerülhetetlen, még ha túl is éli az ember. Megfontolandó tehát a metanol mérgezett emberek oxigénnel való kezelésének megkísérlése, mintha szénmonoxid mérgezésük lenne, amely siker esetén életmentő lehet.
Az oxidációs folyamat vége a kémia és a morfológia szerint is széndioxid és víz, amelyek modelljét és viselkedését a víznél fogjuk majd részletesen bemutatni.
A másik modellezett vegyület az etil-alkohol (etanol, borszesz, alkohol), melynek konvencionális szerkezeti képlete C2H5OH. Morfológiailag az összetevői: 1O, 2C, 6H. A modellezendő molekula egy vízzel jól elegyedő, kis viszkozitású, jó oldószer folyadék molekulája, azaz tulajdonságai hasonlóak az előbbiekben modellezett metanolhoz. Attól csak egy szénatomban és két protonban tér el.
A metanol molekula modellezéséhez hasonlóan a hat protont a két szén között elosztva, az oxigént pedig az így létrejött két metil között elhelyezve kapjuk a következő két lehetséges morfológiai változatot.
Kép + Avogadro fájl
Kép + Avogadro fájl
A folyadéknak jobban megfelelne a hidrogén-híd kötéses változat, azonban a 3-3 kötéssel kapcsolt változat is folyadékot alkot (szabad kapcsolódási helyei alapján), ezért nem dönthető el ennyiből, hogy melyik a helyes modell. De minket most nem is maga az alkohol, hanem annak az emberi szervezetben keletkező metabolitja, és annak a hatása érdekel.
Úgy tudjuk, hogy az etilalkoholból oxidációval acetaldehid (C2H4O) keletkezik. Morfológiailag ennek összetevői: 1O, 2C, 4H. Ha a 4 protont az előbbi eljárásnak megfelelően (a formai kiegészülés összefüggése szerint) páronként elosztva elhelyezzük a két szén csonka (tehát kiegészülő) csúcsán, formailag két nitrogén 14-et kapunk. (lásd fentebb) Ha most a két morfológiai nitrogént (metilént) két oldalról az oxigénhez kapcsoljuk, ugyanazzal a kötéssel, mint a monoxidnál tettük, akkor a következő formájú molekulát kapjuk az acetaldehidre.
Kép + Avogadro fájl
Ha a képen látható modellt pusztán morfológiailag értelmezzük, akkor észrevehetjük, hogy az teljesen azonos a dinitrogén oxid molekulával, amelyet kéjgázként is ismerhetünk. Megdöbbentő, hogy a morfológiai modellezéssel milyen összefüggések tárhatók fel az egymástól kémiailag nagyon különbözőnek gondolt két molekula között, amit azok nagyon hasonló hatása egyébként jól igazol. Alappal feltételezhető tehát, hogy a két molekula – a kéjgáz és az alkohol metabolit – ugyanazon mechanizmussal, ugyanazon receptorokon kötődve hat az emberi szervezetre.
De menjünk tovább, és folytassuk az oxidációs sort. Úgy tudjuk, hogy az acetaldehidből további oxidációval ecetsav (etánsav, metánkarbonsav, acetil-hidroxid vagy hidrogén acetát) keletkezik. Ennek szerkezeti képlete: CH3COOH, amely morfológiailag 2O, 2C, 4H-t jelent, azaz az előbb modellezett acetaldehid oxidja oly módon, hogy az egyik morfológiai nitrogén allotróp (metil) másik végéhez is kapcsolódik egy oxigén atom. A modell így néz ki.
Kép + Avogadro fájl
Láthatjuk, hogy a keletkezett molekula képes a vízzel kémiai oldódással elegyedni. Egyik végén ugyanis egy „kiálló”, csúcshelyzetű protonja van, amely hidrogén hídként képes egy vízmolekulával kötődni. A másik végén pedig egy oxigén van, amely a vízmolekulához annak a hidrogénjén osztozva képes kapcsolódni. A folyamat vége valószínűleg itt is széndioxid és víz lesz, amelyeket a víznél fogunk részletesen tárgyalni.
Folytatása következik. (glicerin, etilén-glikol, izopropil alkohol, stb.)


 Téma:
Téma:  Címkék:
Címkék: